Zusatzinformationen
Endosporen | Sterilisationsverfahren | Theorie | Verbandstoffe | Hinweise zum Autoklavenbetrieb
Es gibt zwar thermophile Bakterien wie Pyrococcus furiosus, die bei 115°C überleben können. Die allermeisten Keime werden jedoch bei solchen Temperaturen abgetötet. Doch warum werden dann beim Autoklavieren 121°C und 1 bar Wasserdampfüberdruck angewendet?
Viele sogenannten mesophilen Bakterien, deren vegetative Zellen bis zu Temperaturen von 60°C wachsen, bilden Endosporen. Das sind sehr stabile Dauerformen, die eine besondere Resistenz gegenüber hohen Temperaturen, Chemikalien und Austrocknung besitzen. Sie können sich im NUGI-Versuch zur Anreicherung eines aeroben Endosporenbildners selbst davon überzeugen.
Wasserdampf wird genutzt, weil er eine wesentlich bessere Wärmeleitfähigkeit besitzt als Luft. Daher müssen beim Trockensterilisieren in Luft wesentlich höhere Temperaturen bei langen Inkubationszeiten verwendet werden, um den gleichen Effekt wie beim Autoklavieren zu erzielen.
Endosporen
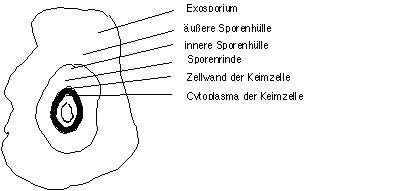
Endosporen werden von einigen Bakterienarten bei ungünstigen Wachstumsbedingungen gebildet. Im mikroskopischen Bild sind sie als doppelt-lichtbrechende (= im Hellfeld "dunkle") Einschlüsse in Zellen, oder als einzelne Objekte sichtbar. In Zellen sind sie an verschiedenen Stellen positioniert, was als Identifikationsmerkmal verwendet wird.
Abbildung 1: Lagen von Endosporen in vegetativen Zellen. Links: terminal, Mitte: subterminal, rechts: zentral.
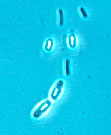
Abbildung 2: Originalaufnahme von Bacillus-Sporen im Lichtmikroskop. Die hellen Bereiche sind die Endosporen, die dunklen Stäbchen sind die vegetativen Bacillus-Zellen.
Endosporen enthalten alle Komponenten einer vegetativen Zelle. Sie besitzen aber im Gegensatz zur vegetativen Zelle (>80% Wasser) einen geringeren Wassergehalt von nur ca. 13% Wasser. Der geringe Wassergehalt reduziert die Stoffwechselaktivitäten und trägt zur Hitzeresistenz der Endosporen bei. Weiterhin stabilisierend soll in Sporenwänden ein Calciumkomplex der Dipicolinsäure wirken, die bisher nur in Endosporen nachgewiesen wurde.
Abbildung 3: Strukturformel von Dipicolinsäure, einer Verbindung aus der Wand von Endosporen.
Als Signal zum Auskeimen der Endosporen können mäßige Hitze oder der Transfer in Vollmedien wirken. Endosporen kommen bei verschiedenen Gram-positiven Genera vor: bei aerobem Bacillus, Sporolactobacillus und Sporosarcina sowie bei anaeroben Clostridium, Desulfotomaculum und Sporomusa.

Abbildung 4: Kolonie des Bacillus cereus var. mycoides auf einer Agarplatte. Typischerweise gibt es "links-" oder "rechtsdrehende" Stämme.
Praktische Konsequenzen aus der Existenz der Endosporen: Wenn Sterilität von Gegenständen und Medien vorausgesetzt wird, so müssen Verfahren angewandt werden, die Endosporen sicher abtöten. So muss entweder bei hohen Temperaturen autoklaviert werden, oder ein hitzeempfindliches Sterilgut wird pasteurisiert bzw. tyndallisiert (= wiederholtes behandeln mit geringerer Temperatur).
Zur Endosporen-Morphologie siehe die folgende Abbildung. Es ist zu beachten, dass die Exosporen, wie sie z.B. bei Actinomyceten vorkommen, nicht diese Hitze- und Chemikalienresistenz besitzen.
Sterilisationsverfahren
| Tabelle 2: Übersicht zu Sterilisationsverfahren | ||
| physikalische Verfahren | Bedingungen | Anmerkung |
| ausglühen | Bunsenbrenner, oxidierender Flammenteil | Impföse, etc. |
| feuchte Hitze | 15 min, 121°C, 1 bar Wasserdampfüberdruck | "autoklavieren" |
| pasteurisieren | Trinkmilch: 71-74°C, 40 sec | Objekt-abhängige Temperaturstufen |
| tyndallisieren | an 3 aufeinanderfolgenden Tagen für 20 min bei 100°C | Hitze als Signal zum Auskeimen der Endosporen, abtöten der daraus entsandenen vegetativen Zellen |
| trockene Hitze | 160°C für 2 Stunden, oder 180°C für 30 min | keine Watte, Papier oder Zellestoff! Parafinöl und Glycerin werden 2 Std. bei 180°C sterilisiert. |
| Sterilfilter | Membranen mit 0,2 µm Porendurchmesser; | Oberflächenfilter z.B. für Antibiotika, Vitamin und Zucker |
| Wattestopfen | Tiefenfilter z.B. für Gase | |
| Strahlen | nicht-ionisierende UV-Strahlung bei 260-280 nm oder bei 185 nm | keine Eindringtiefe! nur für Oberflächenbehandlung; bei 185 nm wird Ozon gebildet |
| ionisierende Gammastrahlung (z.B. 60Co) | Strahlenschutz beachten, bei temperaturempfindlichen medizinischen Gütern | |
| chemische Verfahren | ||
| Ethylenoxid | 90% Ethylenoxid + 10% CO2 für mehrere Stunden | Explosionsgefahr, Rückstände können ätzend sein; für temperaturempfindliche medizinische Güter |
| Alkohole | 70% Ethanol oder Isopropanol | je längerkettig der Alkohol, desto geringer kann seine Wirkstoffmenge sein, denaturiert Proteine und die Cytoplasmamembran. |
| Phenole | töten keine Endosporen ab; sind hautresorbierbar | |
| Aldehyde | <1% | z.B. Formaldehyd, reagiert bevorzugt mit NH2-, SH- und OH-Gruppen |
| Halogene | HOCl unterchlorige Säure | stark oxidierend, chloriert organische Verbindungen |
| Oxidationsmittel | Peressigsäure 0,0025% für <5 min, H2O2, Jodtinktur, Ozon | stark korrosiv, H2O2 wird durch Katalase inaktiviert, Jodid jodiert aromatische Aminosäuren (Tyr), Ozon für die Trinkwasserbehandlung |
| Detergenzien | z.B. Spülmittel, ändern die Cytoplasmamembranen | |
| Säuren | Essigsäure, Milchsäure, Benzoesäure- und Derivate in der Lebensmitteltechnologie | |
Physikalische Verfahren sind auf die Deponierung von Energie im Sterilgut ausgelegt. Chemische Verfahren basieren auf Desinfektionsmittel, die häufig Oxidations- oder Alkylierungsreaktionen bewirken. Die Desinfektionsmittel sollten optimalerweise folgende Kriterien erfüllen:
- ausreichende Wirksamkeit besitzen: Keimreduktion um 99,999%, also von 106 auf maximal 10 lebensfähige Keime!
- toxikologisch unbedenklich sein: nicht mutagen oder cancerogen
- ökologisch unbedenklich und biologisch leicht abbaubar
- ausreichende Lagerstabilität und Materialverträglichkeit
- bei Hautdesinfektion: gute Hautverträglichkeit
Häufige Desinfektionsmittel sind Alkohole, deren Wirksamkeit (denaturieren von Proteinen und Membranen) von ihrer Alkylkettenlänge abhängt. Langkettige Alkohole sind wirksamer als kurzkettige: das Optimum wird bei 2-Ethylhexanol erreicht. Alkohole zeigen geringe Hautresorption; sie sind umweltverträglich aber leicht entzündlich; sie sind kaum wirksam gegen unbehüllte Viren und Endosporen. Als Hautdesinfektionsmittel werden sie in Kombination mit 0.1% Octenidindihydrochlorid eingesetzt, das eine bessere Langzeitwirkung besitzt und die Wiederbesiedlung für einige Zeit verhindert.
Theorie
Messungen mit Endosporen ergaben, dass während des Autoklavierens die Anzahl lebensfähiger Keime exponentiell abnimmt. Die Abnahme pro Zeiteinheit ist keim- und verfahrensspezifisch. Die charakteristische Kenngröße für diesen Prozess ist der D-Wert.
Der D-Wert gibt die Zeit an, innerhalb der die Zahl lebensfähiger Keime auf 1/10 der Ausgangskeimzahl abgenommen hat. Rechnerisch also:
Durch Integration erhält man:
Logarithmieren ergibt:
Daraus ergibt sich: ln 1/10 = - k D und folglich ein D-Wert von D121 = 1,5 - 4,0 min. Dieses Ergebnis bedeutet: nach 1,5 bis 4 min sind nur noch 10% aller Endosporen lebensfähig.
D-Werte wurden für mehrere Bakteriensporen unter verschiedenen experimentellen Bedingungen gemessen. Prinzipiell sind D-Werte theoretisch. Sie werden für verschiedene Sterilisationsverfahren mit Referenzorganismen bestimmt.
| Tabelle 3: Referenzorganismen zur Prüfung von Sterilisationsverfahren | |
| Bacillus stearothermophilus | Dampfsterilisation |
| Bacillus pumilus | Gammastrahlensterilisation |
| Bacillus subtilis | Ethylenoxidbehandlung |
Sterilisation von Verbandstoffen
Drei Verfahren sind üblich: Autoklavieren, Gassterilisation, Sterilisation durch ionisierende Strahlen.
1. Verfahren: Autoklavieren
In Krankenhäusern wird häufig mit gespanntem Wasserdampf von 134°C = 2 bar Überdruck gearbeitet, da so mit einer rascheren Keimabtötung als bei 120°C = 1 bar Überdruck zu rechnen ist. Nach Vorgaben des Arzneibuches wird das Sterilgut 20 min bei 121°C, oder 5 min bei 134°C inkubiert.
2. Verfahren: Gassterilisation mit Ethylenoxid
Ein Beispiel für ein chemisches Sterilisierungsmittel ist Ethylenoxid (Abbildung 3). Dieses Gas wird häufig für die Sterilisation temperaturempfindlicher Gegenstände in der Medizin genutzt.
Abbildung 3: Strukturformel des Ethylenoxids.
Die Ringspannung des Moleküls erklärt seine Reaktivität. Achtung: explosive Luftgemische, entflammbar! Hydrolysiert in Wasser, was durch Säure beschleunigt wird. Ist ein Alkylierungsmittel, das mit OH- und NH2-Gruppen reagieren kann.
Der Erfolg des Verfahrens hängt von der Gaskonzentration, der relativen Luftfeuchtigkeit und der Einwirkdauer ab: Luft wird abgepumpt, dann mit leichtem Überdruck das Sterilisationsgas (10 % Ethylenoxid in 90% CO2 bei 50-60% relativer Luftfeuchte) zugeleitet und 12-15 Std. inkubiert. Zur Wirkungsweise des Ethylenoxids: Die Ringspannung macht Ethylenoxid reaktiv. Ethylenoxid alkyliert Proteine, bzw. verestert Säuren oder führt zu einer Ether- bzw. Thioetherbildung mit entsprechenden funktionellen Gruppen.
Nachteile der Gassterilisation:
Gemische von 3% Ethylenoxid in Luft sind explosiv.
Alle Gasreste müssen entfernt sein, da sonst Hautreizungen auftreten können.
100 - 200 mg Ethylenoxid pro Liter Luft wirken beim Menschen innerhalb kurzer Zeit tödlich.
3. Verfahren: Sterilisation mit ionisierenden Strahlen
Zum Einsatz kommen Elektronenbeschleuniger und Gammastrahlen. Gamma-Strahlen sind wegen der größeren Eindringtiefe gegenüber dem Elektronenbeschleuniger zu bevorzugen!
Als Strahlenquellen werden 60Co und 137Cäsium mit 100 000 bis 300 000 Curie Radioaktivität verwendet. Für sicheres Abtöten von vegetativen Zellen und Endosporen sollte eine Strahlendosis von 2,5 - 3 Mrad (Megarad = 106 rad) auf das Sterilisationsgut einwirken. Strahlensterilisiert werden neben vielen medizinischen Materialien u.a. Plastikpetrischalen und Gewürze.
Nachteile des Verfahrens: Es ist teuer und verlangt besondere Sicherheitsmaßnahmen wegen der Strahlenquellen.
Hinweis zum Autoklavenbetrieb
- Der Betreiber eines Autoklaven ist nach Druckbehälterverordnung für eine regelmäßige Kontrolle des Gerätes durch eine sachkundige Person verantwortlich. In der Regel sollte eine solche Untersuchung einmal jährlich stattfinden.
- Sie sollten je nach Häufigkeit des Autolavengebrauches seine Funktionsweise durch einen zugelassenen Bioindikator überprüfen.
- Als Bioindikator werden in der Regel Endosporen von Bacillus stearothermophilus in Ampullen mit Nährmedium verwendet. Befolgen Sie die Herstellerangaben. In der Regel werden sie wie folgt aussehen: Eine Bioindikatorampulle wird einem normalen Autoklaviervorgang beigelegt. Anschließend werden die Ampullen bei 65°C bebrütet, der optimalen Wachstumstemperatur dieses Bakteriums. Bleibt die Färbung des Indikator unverändert, dann funktioniert Ihr Autoklav ausreichend.